IA para Estratificação de Risco: Modelos DL Multimodais Oferecem Prognóstico Melhorado para Embolia Pulmonar
Tabela de Links
Resumo
- Introdução
- Métodos
- Resultados
- Discussão
- Conclusões, Agradecimentos e Referências
5. Conclusões
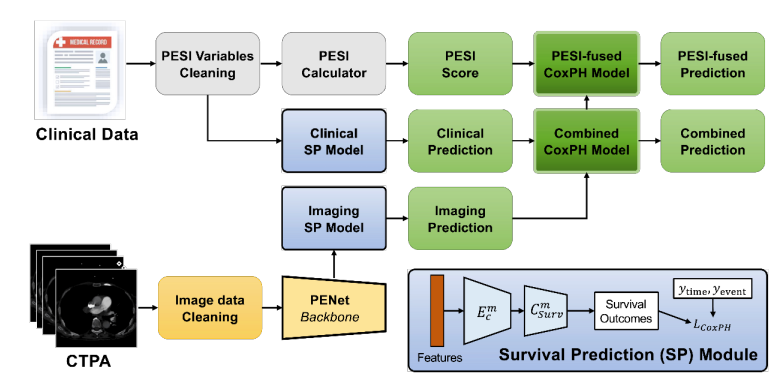
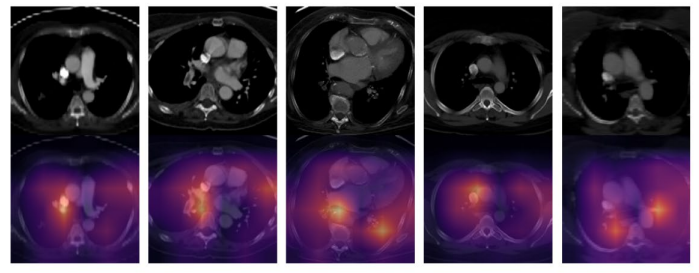
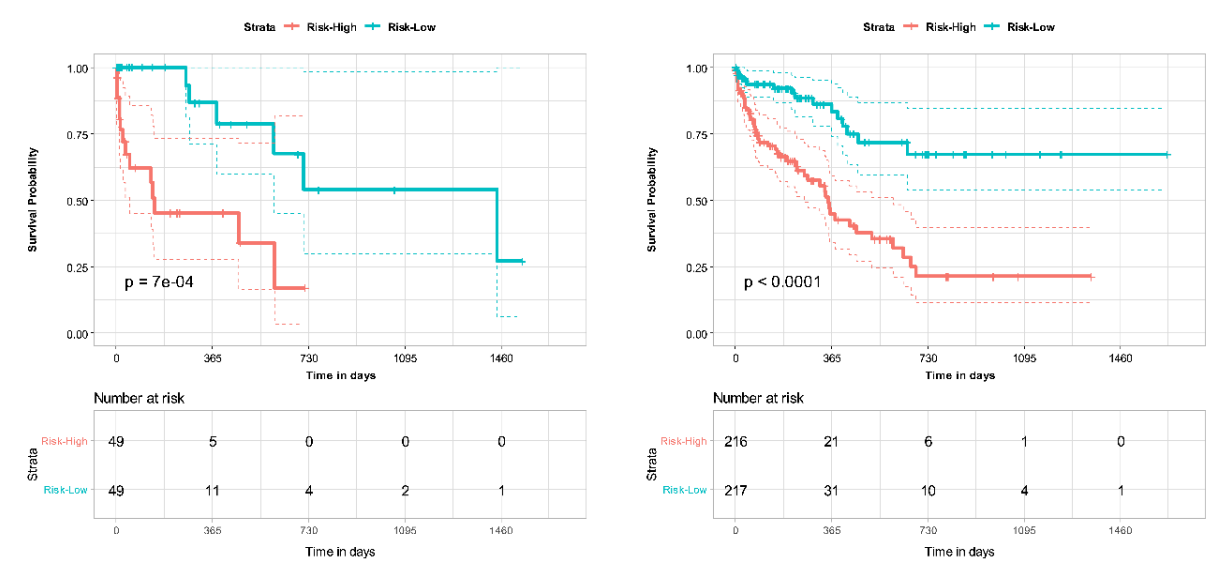
Os modelos DL multiómicos baseados em características CTPA combinadas e variáveis clínicas demonstraram desempenho melhorado em comparação com a pontuação PESI isolada para previsão de mortalidade na EP. A adição do PESI ao modelo multimodal demonstrou apenas uma melhoria marginal no desempenho, ilustrando que os modelos baseados em IA são suficientemente capazes de prever a sobrevivência. Os modelos multimodais melhoraram de forma semelhante o desempenho em relação ao PESI isolado na estimativa de risco de mortalidade em 30 dias. Através da análise NRI, os dados clínicos e de imagem demonstraram independentemente contribuir para o melhor desempenho do modelo multimodal. Estas descobertas demonstram a força de um modelo DL multimodal em comparação com o padrão clínico atual do PESI, transformando o prognóstico num processo inteligente que integra maior informação clínica e de imagem. Adicionalmente, demonstrámos a concordância do nosso modelo com indicadores clínicos de mortalidade, como a disfunção do VD. Análises adicionais podem esclarecer melhor a conexão de vários fatores de risco com a mortalidade em pacientes com EP, e como esta informação pode ser aproveitada para o desenvolvimento de modelos na previsão de sobrevivência. No entanto, os benefícios do nosso modelo só podem ser confirmados por validação adicional em conjuntos de dados maiores e mais diversos, bem como por testes prospetivos dos modelos desenvolvidos.
\ O nosso estudo destaca a utilidade dos modelos baseados em DL no prognóstico e estratificação de risco em pacientes com EP. A IA tem o potencial de melhorar o fluxo de trabalho clínico para radiologistas e médicos, fornecendo informações diagnósticas e prognósticas rápidas e precisas. Ao oferecer uma estratificação de risco oportuna e precisa para pacientes com EP, a IA pode oferecer um benefício substancial aos pacientes e prestadores, informando a tomada de decisão clínica, potencialmente melhorando os resultados dos pacientes.
Agradecimentos
Nenhum.
Referências
-
Beckman MG, Hooper WC, Critchley SE, Ortel TL. Venous thromboembolism: a public health concern. American journal of preventive medicine. 2010;38(4):S495-S501.
\
-
Lewis AE, Gerstein NS, Venkataramani R, Ramakrishna H. Evolving management trends and outcomes in catheter management of acute pulmonary embolism. Journal of Cardiothoracic and Vascular Anesthesia. 2022;36(8):3344-3356.
\
-
Goldhaber SZ, Bounameaux H. Pulmonary embolism and deep vein thrombosis. The Lancet. 2012;379(9828):1835-1846.
\
-
Piazza G, Goldhaber SZ. Acute pulmonary embolism: part I: epidemiology and diagnosis. Circulation. 2006;114(2):e28-e32.
\
-
Aujesky D, Obrosky DS, Stone RA, et al. Derivation and validation of a prognostic model for pulmonary embolism. American journal of respiratory and critical care medicine. 2005;172(8):1041-1046.
\
-
Donzé J, Le Gal G, Fine MJ, et al. Prospective validation of the pulmonary embolism severity index. Thrombosis and haemostasis. 2008;100(05):943-948.
\
-
Ishwaran H, Kogalur UB, Blackstone EH, Lauer MS. Random survival forests. 2008;
\
-
Fox J, Weisberg S. Cox proportional-hazards regression for survival data. An R and S-PLUS companion to applied regression. 2002;2002
\
-
Katzman JL, Shaham U, Cloninger A, Bates J, Jiang T, Kluger Y. DeepSurv: personalized treatment recommender system using a Cox proportional hazards deep neural network. BMC medical research methodology. 2018;18(1):1-12.
\
-
Oren O, Gersh BJ, Bhatt DL. Artificial intelligence in medical imaging: switching from radiographic pathological data to clinically meaningful endpoints. The Lancet Digital Health. 2020;2(9):e486-e488.
\
-
Weikert T, Winkel DJ, Bremerich J, et al. Automated detection of pulmonary embolism in CT pulmonary angiograms using an AI-powered algorithm. European radiology. 2020;30:6545-6553.
\
-
Huang S-C, Kothari T, Banerjee I, et al. PENet—a scalable deep-learning model for automated diagnosis of pulmonary embolism using volumetric CT imaging. NPJ digital medicine. 2020;3(1):61.
\
-
Huang S-C, Pareek A, Zamanian R, Banerjee I, Lungren MP. Multimodal fusion with deep neural networks for leveraging CT imaging and electronic health record: a case-study in pulmonary embolism detection. Scientific reports. 2020;10(1):22147.
\
-
Liu W, Liu M, Guo X, et al. Evaluation of acute pulmonary embolism and clot burden on CTPA with deep learning. European radiology. 2020;30:3567-3575.
\
-
Yao J, Zhu X, Zhu F, Huang J. Deep correlational learning for survival prediction from multi-modality data. Springer; 2017:406-414.
\
-
Vale-Silva LA, Rohr K. Long-term cancer survival prediction using multimodal deep learning. Scientific Reports. 2021;11(1):13505.
\
-
Meyer G, Vicaut E, Danays T, et al. Fibrinolysis for patients with intermediate-risk pulmonary embolism. New England Journal of Medicine. 2014;370(15):1402-1411.
\
-
Hofmanninger J, Prayer F, Pan J, Röhrich S, Prosch H, Langs G. Automatic lung segmentation in routine imaging is primarily a data diversity problem, not a methodology problem. European Radiology Experimental. 2020;4(1):1-13.
\
-
Harrell Jr FE, Lee KL, Califf RM, Pryor DB, Rosati RA. Regression modelling strategies for improved prognostic prediction. Statistics in medicine. 1984;3(2):143-152.
\
-
Leening MJ, Vedder MM, Witteman JC, Pencina MJ, Steyerberg EW. Net reclassification improvement: computation, interpretation, and controversies: a literature review and clinician's guide. Annals of internal medicine. 2014;160(2):122-131.
\
-
Kaplan EL, Meier P. Nonparametric estimation from incomplete observations. Journal of the American statistical association. 1958;53(282):457-481.
\
-
Grifoni S, Olivotto I, Cecchini P, et al. Short-term clinical outcome of patients with acute pulmonary embolism, normal blood pressure, and echocardiographic right ventricular dysfunction. Circulation. 2000;101(24):2817-2822.
\
-
Coutance G, Cauderlier E, Ehtisham J, Hamon M, Hamon M. The prognostic value of markers of right ventricular dysfunction in pulmonary embolism: a meta-analysis. Critical care. 2011;15:1-10.
\
-
Chaudhary K, Poirion OB, Lu L, Garmire LX. Deep learning–based multi-omics integration robustly predicts survival in liver cancer. Clinical Cancer Research. 2018;24(6):1248-1259.
\
-
Somani SS, Honarvar H, Narula S, et al. Development of a machine learning model using electrocardiogram signals to improve acute pulmonary embolism screening. European Heart Journal-Digital Health. 2022;3(1):56-66.
\
-
Tourassi GD, Floyd CE, Sostman HD, Coleman RE. Acute pulmonary embolism: artificial neural network approach for diagnosis. Radiology. 1993;189(2):555-558.
\
-
Soffer S, Klang E, Shimon O, et al. Deep learning for pulmonary embolism detection on computed tomography pulmonary angiogram: a systematic review and meta-analysis. Scientific reports. 2021;11(1):15814.
\
-
Elias A, Mallett S, Daoud-Elias M, Poggi J-N, Clarke M. Prognostic models in acute pulmonary embolism: a systematic review and meta-analysis. BMJ open. 2016;6(4):e010324.
\
-
Cahan N, Klang E, Marom EM, et al. Multimodal fusion models for pulmonary embolism mortality prediction. Scientific Reports. 2023;13(1):1-15.
Figura
\ 
\ 
\ 
\ 
\ 
\ 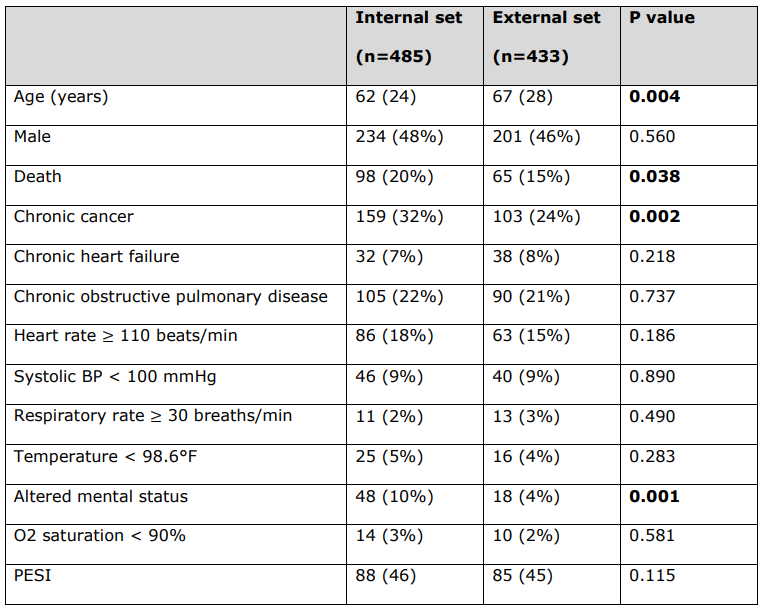
\ Características detalhadas dos pacientes das variáveis clínicas PESI utilizadas para calcular a pontuação PESI para cada paciente.
\ Todas as variáveis contínuas são relatadas como mediana (intervalo interquartil), e todas as variáveis categóricas são relatadas como número (%). Valores p estatisticamente significativos estão em negrito (p < 0,05). O estado de falecido não é uma variável clínica PESI.
\ BP = Pressão Arterial. PESI = Índice de Severidade da Embolia Pulmonar.
\ 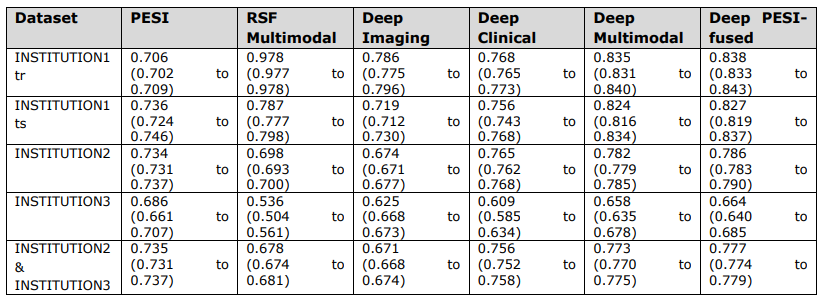
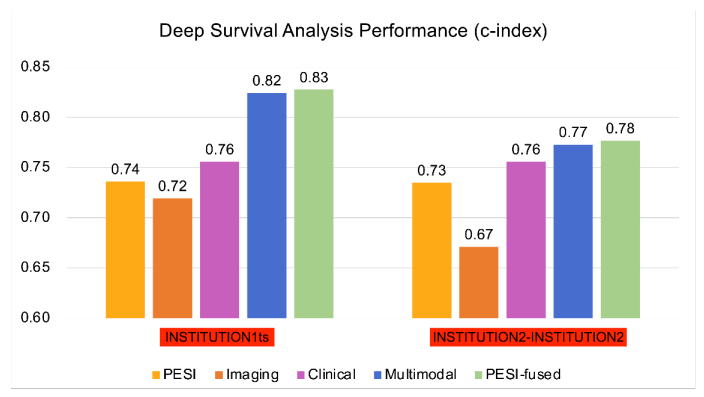
\ Valores gerais do índice c e intervalos de confiança de 95% correspondentes do PESI e modelos de previsão.
\ INSTITUTION3 = INSTITUTION3. PESI = Índice de Severidade
Você também pode gostar

Ascensão do Bitcoin Ligada a Aberturas Diplomáticas e Redução de Tensões

Nhà đầu tư rút vốn khỏi ETH dù mạng Ethereum tăng trưởng mạnh?






